Хлорная коррозия труб в котлах
Коррозия в котлах




 Виды коррозии. В процессе работы элементы парового котла подвергаются воздействию агрессивных сред — воды, пара и дымовых газов. Различают коррозию химическую и электрохимическую.
Виды коррозии. В процессе работы элементы парового котла подвергаются воздействию агрессивных сред — воды, пара и дымовых газов. Различают коррозию химическую и электрохимическую.
Химическая коррозия ,вызванная паром или водой, разрушает металл равномерно по всей поверхности. Скорость такой коррозии в современных судовых котлах низкая. Более опасна местная химическая коррозия, вызываемая агрессивными химическими соединениями, содержащимися в отложениях золы (серы, окислов ванадия и т. п.).
Наиболее распространенной и опасной является электрохимическая коррозия , протекающая в водных растворах электролитов при возникновении электрического тока, вызванного разностью потенциалов между отдельными участками металла, отличающимися химической неоднородностью, температурой или качеством обработки.
Роль электролита выполняют вода (при внутренней коррозии) или сконденсировавшиеся пары воды в отложениях (при наружной коррозии).
Возникновение таких микрогальванических пар на поверхности труб приводит к тому, что ион-атомы металла переходят в воду в виде положительно заряженныхионов, а поверхность трубы в этом месте приобретает отрицательный заряд. Если различие в потенциалах таких микрогальванических пар незначительно, то на границе металл-вода постепенно создается двойной электрический слой, который тормозит дальнейший ход процесса.
Однако в большинстве случаев потенциалы отдельных участков различны, что обусловливает возникновение ЭДС, направленной от большего потенциала (анода) к меньшему (катоду).
При этом с анода в воду переходят ион-атомы металла, а на катоде накапливаются избыточные электроны. В результате ЭДС и, следовательно, интенсивность процесса разрушения металла резко снижаются.
Это явление называется поляризацией. Если потенциал анода уменьшается в результате образования защитной оксидной пленки или роста концентрации ионов металла в районе анода, а потенциал катода практически не изменяется, то поляризация носит название анодной.
При катодной поляризации в растворе у катода резко падает концентрация ионов и молекул, способных удалять избыточные электроны с поверхности металла. Из этого следует, что основным моментом борьбы с электрохимической коррозией является создание таких условий, когда будут поддерживаться оба вида поляризации.
Практически достигнуть этого невозможно, так как в котловой воде всегда имеются деполяризаторы — вещества, вызывающие нарушение процессов поляризации.
К деполяризаторам относятся молекулы О2 и СО2, ионы Н + , Сl — и SO — 4, а также окислы железа и меди. Растворенные в воде СО2, Cl — и SO — 4 тормозят образование на аноде плотной защитной оксидной пленки и тем самым способствуют интенсивному протеканию анодных процессов. Ионы водорода Н + снижают отрицательный заряд катода.
Влияние кислорода на скорость коррозии стало проявляться в двух противоположных направлениях. С одной стороны, кислород увеличивает скорость коррозионного процесса, так как является сильным деполяризатором катодных участков, с другой оказывает пассивирующее действие на поверхность.
Обычно детали котла, изготовленные из стали, имеют достаточно прочную первоначальную оксидную пленку, которая защищает материал от воздействия кислорода до тех пор, пока не будет разрушена под действием химических или механических факторов.
Скорость гетерогенных реакций (к которым относится и коррозия) регулируется интенсивностью следующих процессов: подводом к поверхности материала реагентов (в первую очередь деполяризаторов); разрушением защитной оксидной пленки; удалением продуктов реакции от места ее протекания.
Интенсивность же этих процессов во многом определяется гидродинамическими, механическими и тепловыми факторами. Поэтому меры по снижению концентрации агрессивных химических реагентов при высокой интенсивности двух других процессов, как показывает опыт эксплуатации котлов, обычно малоэффективны.
Отсюда следует, что решение проблемы предотвращения коррозионных повреждений должно быть комплексным, когда учитываются все факторы, влияющие на исходные причины разрушения материалов.
В зависимости от места протекания иучаствующих в реакциях веществ различают следующие виды электрохимической коррозии:
- кислородную (и ее разновидность — стояночную),
- подшламовую (иногда называемую „ракушечной»),
- межкристаллитную (щелочная хрупкость котельных сталей),
- щелевую и
- сернистую.
Кислородная коррозия наблюдается в экономайзерах, арматуре, питательных и опускных трубах, пароводяных коллекторах и внутриколлекторных устройствах (щитах, трубах, пароохладителях и т.п.). Особенно сильно подвержены кислородной коррозии змеевики второго контура двухконтурных котлов, утилизационных котлов и паровых воздухоподогревателей. Кислородная коррозия протекает во время действия котлов и зависит от концентрации кислорода, растворенного в котловой воде.
Скорость кислородной коррозии в главных котлах низкая, что обусловлено эффективной работой деаэраторов и фосфатно-нитратным водным режимом. Во вспомогательных водотрубных котлах она нередко достигает 0,5 — 1 мм/год, хотя в среднем лежит в пределах 0,05 — 0,2 мм/год. Характер повреждения котельных сталей — язвы небольших размеров.
Более опасной разновидностью кислородной коррозии является стояночная коррозия , протекающая в период бездействия котла. В силу специфики работы все судовые котлы (а вспомогательные особенно) подвержены интенсивной стояночной коррозии. Как правило, стояночная коррозия не приводит к отказам котла, однако металл, подвергшийся коррозии во время остановок, при прочих равных условиях более интенсивно разрушается при работе котла.
Основной причиной возникновения стояночной коррозии является попадание кислорода в воду, если котел заполнен, или в пленку влаги на поверхности металла, если котел осушен. Большую роль при этом играют хлориды и NaOH, содержащиеся в воде, и водорастворимые отложения солей.
При наличии в воде хлоридов интенсифицируется равномерная коррозия металла, а если в ней содержится незначительное количество щелочей (меньше 100 мг/л), то коррозия локализуется. Чтобы избежать стояночной коррозии при температуре 20 — 25 °С в воде должно содержаться до 200 мг/л NaOH.
Внешние признаки коррозии с участием кислорода: локальные язвы небольшого размера (рис. 1, а), заполненные продуктами коррозии бурого цвета, которые образуют бугорки над язвами.
Удаление кислорода из питательной воды является одним из важных мероприятий по снижению кислородной коррозии. С 1986 г. содержание кислорода в питательной воде для судовых вспомогательных и утилизационных котлов ограничивается 0,1 мг/л.
Однако и при таком кислородосодержании питательной воды в эксплуатации наблюдаются коррозионные повреждения элементов котла, что свидетельствует о преобладающем влиянии процессов разрушения оксидной пленки и вымывании продуктов реакции из очагов коррозии. Наиболее наглядным примером, иллюстрирующим влияние этих процессов на коррозионные повреждения, являются разрушения змеевиков утилизационных котлов с принудительной циркуляцией.
Рис. 1. Повреждения при кислородной коррозии
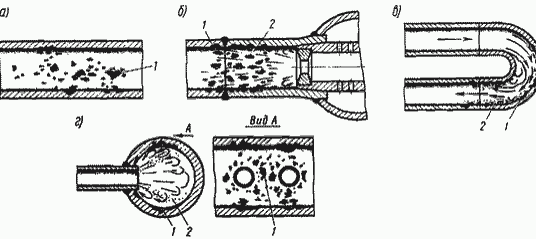
Коррозионные повреждения при кислородной коррозии обычно строго локализованы: на внутренней поверхности входных участков (см. рис. 1, а), в районе гибов (рис. 1, б), на выходных участках и в колене змеевика (см. рис. 1, в), а также в пароводяных коллекторах утилизационных котлов (см. рис. 1, г). Именно на этих участках (2 — область пристенной кавитации) гидродинамические особенности потока создают условия для разрушения оксидной пленки и интенсивного вымывания продуктов коррозии.
Действительно, любые деформации потока воды и пароводяной смеси сопровождаются возникновением кавитации в пристенных слоях расширяющегося потока 2, где образующиеся и тут же схлопывающиеся пузырьки пара обусловливают разрушение оксидной пленки вследствие энергии гидравлических микроударов.
Этому способствуют также знакопеременные напряжения в пленке, вызванные вибрацией змеевиков и колебаниями температуры и давлений. Повышенная же локальная турбулизация потока на этих участках вызывает активное вымывание продуктов коррозии.
На прямых выходных участках змеевиков оксидная пленка разрушается из-за ударов о поверхность капелек воды при турбулентных пульсациях потока пароводяной смеси, дисперсно-кольцевой режим движения которой переходит здесь в дисперсный при скорости потока до 20-25 м/с.
В этих условиях даже невысокое кислородосодержание (
0,1 мг/л) обусловливает интенсивное разрушение металла, что приводит к появлению свищей на входных участках змеевиков утилизационных котлов типа Ла Монт через 2-4 года эксплуатации, а на остальных участках — через 6-12 лет.
Рис. 2. Коррозионные повреждения змеевиков экономайзеров утилизационных котлов КУП1500Р теплохода «Индира Ганди».
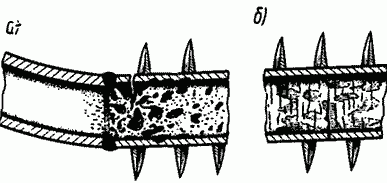
В качестве иллюстрации к изложенному рассмотрим причины повреждения змеевиков экономайзеров двух утилизационных котлов типа КУП1500Р, установленных на лихтеровозе «Индира Ганди» (типа «Алексей Косыгин»), который вступил в эксплуатацию в октябре 1985 г. Уже в феврале 1987 г. из-за повреждений заменены экономайзеры обоих котлов. Через 3 года и в этих экономайзерах появляются повреждения змеевиков, расположенные на участках до 1-1,5 м от входного коллектора. Характер повреждений свидетельствует (рис. 2, а, б) о типичной кислородной коррозии с последующим усталостным разрушением (поперечные трещины).
Однако природа усталости на отдельных участках различна. Появление трещины (а ранее — растрескивание оксидной пленки) в районе сварного шва (см. рис. 2, а) является следствием знакопеременных напряжений, обусловленных вибрацией пучка труб и конструктивной особенностью узла соединения змеевиков с коллектором (к изогнутому штуцеру диаметром 22×3 приварен конец змеевика диаметром 22×2).
Разрушение же оксидной пленки и образование усталостных трещин на внутренней поверхности прямых участков змеевиков, удаленных от входа на 700-1000 мм (см. рис. 2, б), обусловлены знакопеременными термическими напряжениями, возникающими в период ввода котла в действие, когда на горячую поверхность подается холодная вода. При этом действие термических напряжений усиливается тем, что оребрение змеевиков затрудняет свободное расширение металла трубы, создавая дополнительные напряжения в металле.
Подшламовая коррозия обычно наблюдается в главных водотрубных котлах на внутренних поверхностях экранных и парообразующих труб притопочных пучков, обращенных к факелу. Характер подшламовой коррозии — язвы овальной формы с размером по большой оси (параллельной оси трубы) до 30-100 мм.
На язвах имеется плотный слой окислов в виде „ракушек» 3 (рис. 3). Подшламовая коррозия протекает в присутствии твердых деполяризаторов — окислов железа и меди 2, которые осаждаются на наиболее теплонапряженных участках труб в местах активных центров коррозии, возникающих при разрушении оксидных пленок.
Сверху образуется рыхлый слой накипи и продуктов коррозии 1. Образующиеся „ракушки» из продуктов коррозии прочно сцеплены с основным металлом и могут быть удаленытолько механическим путем. Под „ракушками» ухудшается теплообмен, что приводит к перегреву металла и появлению выпучин.
Для вспомогательных котлов этот вид коррозии не характерен, но при высоких тепловых нагрузках и соответствующих режимах водообработки не исключено появление подшламовой коррозии и в этих котлах.
Лестницы. Входная группа. Материалы. Двери. Замки. Дизайн
Хлорная коррозия труб в котлах. Коррозионные повреждения экранных труб газомазутных котлов. Щелочная хрупкость стали
Корро́зия (от лат. corrosio — разъедание) — это самопроизвольное разрушение металлов в результате химического или физико-химического взаимодействия с окружающей средой. В общем случае это — разрушение любого материала — будь то металл или керамика, дерево или полимер. Причиной коррозии служит термодинамическая неустойчивость конструкционных материалов к воздействию веществ, находящихся в контактирующей с ними среде. Пример — кислородная коррозия железа в воде:
4Fe + 2Н 2 О + ЗО 2 = 2(Fe 2 O 3 Н 2 О)
В повседневной жизни для сплавов железа (сталей) чаще используют термин «ржавление». Менее известны случаи коррозии полимеров. Применительно к ним существует понятие «старение», аналогичное термину «коррозия» для металлов. Например, старение резины из-за взаимодействия с кислородом воздуха или разрушение некоторых пластиков под воздействием атмосферных осадков, а также биологическая коррозия. Скорость коррозии, как и всякой химической реакции очень сильно зависит от температуры. Повышение температуры на 100 градусов может увеличить скорость коррозии на несколько порядков.
Коррозионные процессы отличаются широким распространением и разнообразием условий и сред, в которых она протекает. Поэтому нет единой и всеобъемлющей классификации встречающихся случаев коррозии. Главная классификация производится по механизму протекания процесса. Различаются два вида: химическую коррозию и электрохимическую коррозию. В данном реферате подробно рассматривается химическая коррозия на примере судовых котельных установках малых и больших мощностей.
Коррозионные процессы отличаются широким распространением и разнообразием условий и сред, в которых она протекает. Поэтому нет единой и всеобъемлющей классификации встречающихся случаев коррозии.
По типу агрессивных сред, в которых протекает процесс разрушения, коррозия может быть следующих видов:
1) -Газовая коррозия
2) -Коррозия в неэлектролитах
3) -Атмосферная коррозия
4) -Коррозия в электролитах
5) -Подземная коррозия
7) -Коррозия блуждающим током.
По условиям протеканию коррозионного процесса различаются следущие виды:
1) -Контактная коррозия
2) -Щелевая коррозия
3) -Коррозия при неполном погружении
4) -Коррозия при полном погружении
5) -Коррозия при переменном погружении
6) -Коррозия при трении
7) -Коррозия под напряжением.
По характеру разрушения:
Сплошная коррозия, охватывающая всю поверхность:
Локальная(местная) коррозия, охватывающая отдельные участки:
3) -точечная(или питтинг);
1. Химическая коррозия
Представим себе металл в процессе производства металлического проката на металлургическом заводе: по клетям прокатного стана движется раскаленная масса. Во все стороны от нее разлетаются огненные брызги. Это с поверхности металла скалываются частички окалины – продукта химической коррозии, возникающего в результате взаимодействия металла с кислородом воздуха. Такой процесс самопроизвольного разрушения металла из-за непосредственного взаимодействия частиц окислителя и окисляемого металла, называется химической коррозией.
Химическая коррозия — взаимодействие поверхности металла с (коррозионно-активной) средой, не сопровождающееся возникновением электрохимических процессов на границе фаз. В этом случае взаимодействия окисление металла и восстановление окислительного компонента коррозионной среды протекают в одном акте. Например, образование окалины при взаимодействии материалов на основе железа при высокой температуре с кислородом:
4Fe + 3O 2 → 2Fe 2 O 3
При электрохимической коррозии ионизация атомов металла и восстановление окислительного компонента коррозионной среды протекают не в одном акте и их скорости зависят от электродного потенциала металла (например, ржавление стали в морской воде).
При химической коррозии окисление металла и восстановление окислительного компонента коррозионной среды происходят одновременно. Такая коррозия наблюдается при действии на металлы сухих газов (воздуха, продуктов горения топлива) и жидких не электролитов (нефти, бензина и т. д.) и представляет собой гетерогенную химическую реакцию.
Процесс химической коррозии происходит следующим образом. Окислительный компонент внешней среды, отнимая у металла валентные электроны, одновременно вступает с ним в химическое соединение, образуя на поверхности металла пленку (продукт коррозии). Дальнейшее образование пленки происходит за счет взаимной двусторонней диффузии через пленку агрессивной среды к металлу и атомов металла по направлению к внешней среде и их взаимодействия. При этом если образующаяся пленка обладает защитными свойствами, т. е. препятствует диффузии атомов, то коррозия протекает с самоторможением во времени. Такая пленка образуется на меди при температуре нагрева 100 °С, на никеле — при 650, на железе — при 400 °С. Нагрев стальных изделий выше 600 °С приводит к образованию на их поверхности рыхлой пленки. С повышением температуры процесс окисления идет с ускорением.
Наиболее распространенным видом химической коррозии является коррозия металлов в газах при высокой температуре — газовая коррозия. Примерами такой коррозии являются окисление арматуры печей, деталей двигателей внутреннего сгорания, колосников, деталей керосиновых ламп и окисление при высокотемпературной обработке металлов (ковке, прокате, штамповке). На поверхности металлоизделий возможно образование и других продуктов коррозии. Например, при действии сернистых соединений на железе образуются сернистые соединения, на серебре при действии паров йода — йодистое серебро и т. д. Однако чаще всего на поверхности металлов образуется слой оксидных соединений.
Большое влияние на скорость химической коррозии оказывает температура. С повышением температуры скорость газовой коррозии увеличивается. Состав газовой среды оказывает специфическое влияние на скорость коррозии различных металлов. Так, никель устойчив в среде кислорода, углекислого газа, но сильно корродирует в атмосфере сернистого газа. Медь подвержена коррозии в атмосфере кислорода, но устойчива в атмосфере сернистого газа. Хром обладает коррозионной стойкостью во всех трех газовых средах.
Для защиты от газовой коррозии используют жаростойкое легирование хромом, алюминием и кремнием, создание защитных атмосфер и защитных покрытий алюминием, хромом, кремнием и жаростойкими эмалями.
2. Химическая коррозия в судовых паровых котлах.
Виды коррозии. В процессе работы элементы парового котла подвергаются воздействию агрессивных сред — воды, пара и дымовых газов. Различают коррозию химическую и электрохимическую.
Химической коррозии подвержены детали и узлы машин, работающих при высоких температурах, — двигатели поршневого и турбинного типа, ракетные двигатели и т. п. Химическое сродство большинства металлов к кислороду при высоких температурах почти неограниченно, так как оксиды всех технически важных металлов способны растворяться в металлах и уходить из равновесной системы:
2Ме(т) + O 2 (г) 2МеО(т); МеО(т) [МеО] (р-р)
В этих условиях окисление всегда возможно, но наряду с растворением оксида появляется и оксидный слой на поверхности металла, который может тормозить процесс окисления.
Скорость окисления металла зависит от скорости собственно химической реакции и скорости диффузии окислителя через пленку, а поэтому защитное действие пленки тем выше, чем лучше ее сплошность и ниже диффузионная способность. Сплошность пленки, образующейся на поверхности металла, можно оценить по отношению объема образовавшегося оксида или другого какого-либо соединения к объему израсходованного на образование этого оксида металла (фактор Пиллинга-Бэдвордса). Коэффициент a (фактор Пиллинга — Бэдвордса) у разных металлов имеет разные значения. Металлы, у которых a в частности, сведения о коррозии их экранов.
Экраны этих котлов были подвержены коррозии как с наружной, так и с внутренней стороны. Их наружная коррозия описана в предыдущем параграфе этой главы, разрушение же внутренней поверхности труб не похоже ни на один из описанных выше видов коррозии металла
Разъедание происходило в основном с огневой стороны верхней части наклонных труб холодной воронки и сопровождалось появлением коррозионных раковин (рис. 63,а). В дальнейшем число таких раковин увеличивалось, и возникала сплошная полоса (иногда две параллельные. полосы) разъеденного металла (рис. 63,6). Характерным являлось также отсутствие коррозии в зоне сварных стыков.
Внутри труб имелся налет рыхлого шлама толщиной 0,1-0,2 мм, состоявшего в основном из окислов железа и меди. Увеличение коррозионного разрушения металла не сопровождалось увеличением толщины слоя шлама, следовательно, коррозия под слоем шлама не была основной причиной разъедания внутренней поверхности экранных труб.
В котловой воде поддерживался режим чистофосфатной щелочности. Фосфаты вводились в котел не.непрерывно, а периодически.
Большое значение имело то обстоятельство, что температура металла труб периодически резко.повышалась и иногда была выше 600° С (рис. 64). Зона наиболее частого и максимального повышения температуры совпадала с зоной наибольшего разрушения металла. Снижение давления в котле до 140-165 ат (т. е. до давления, при котором работают новые серийные котлы) не изменяло характера временного повышения температуры труб, но сопровождалось значительным снижением максимального значения этой температуры. Причины такого периодического повышения температуры огневой стороны наклонных труб холодной. воронки еще подробно не изучены.

В настоящей книге рассматриваются конкретные вопросы, связанные с работой стальных деталей парового котла. Но для изучения этих сугубо практических вопросов необходимо знать общие сведения, касающиеся строения стали и ее » свойств. В схемах, показывающих строение металлов, атомы иногда изображают в виде соприкасающихся друг с другом шаров (рис. 1). Такие схемы показывают расстановку атомов в металле, но в них трудно наглядно показать расположение атомов друг относительно друга.
Эрозией называется постепенное разрушение поверхностного слоя металла под влиянием механического воздействия. Наиболее распространенным видом эрозии стальных элементов — парового котла является их истирание твердыми частицами золы, движущейся вместе с дымовыми газами. При длительном истирании происходит постепенное уменьшение толщины стенок труб, а затем их деформация и разрыв под действием внутреннего давления.
Лестницы. Входная группа. Материалы. Двери. Замки. Дизайн
Хлорная коррозия труб в котлах. Коррозионные повреждения экранных труб газомазутных котлов. Щелочная хрупкость стали
Корро́зия (от лат. corrosio — разъедание) — это самопроизвольное разрушение металлов в результате химического или физико-химического взаимодействия с окружающей средой. В общем случае это — разрушение любого материала — будь то металл или керамика, дерево или полимер. Причиной коррозии служит термодинамическая неустойчивость конструкционных материалов к воздействию веществ, находящихся в контактирующей с ними среде. Пример — кислородная коррозия железа в воде:
4Fe + 2Н 2 О + ЗО 2 = 2(Fe 2 O 3 Н 2 О)
В повседневной жизни для сплавов железа (сталей) чаще используют термин «ржавление». Менее известны случаи коррозии полимеров. Применительно к ним существует понятие «старение», аналогичное термину «коррозия» для металлов. Например, старение резины из-за взаимодействия с кислородом воздуха или разрушение некоторых пластиков под воздействием атмосферных осадков, а также биологическая коррозия. Скорость коррозии, как и всякой химической реакции очень сильно зависит от температуры. Повышение температуры на 100 градусов может увеличить скорость коррозии на несколько порядков.
Коррозионные процессы отличаются широким распространением и разнообразием условий и сред, в которых она протекает. Поэтому нет единой и всеобъемлющей классификации встречающихся случаев коррозии. Главная классификация производится по механизму протекания процесса. Различаются два вида: химическую коррозию и электрохимическую коррозию. В данном реферате подробно рассматривается химическая коррозия на примере судовых котельных установках малых и больших мощностей.
Коррозионные процессы отличаются широким распространением и разнообразием условий и сред, в которых она протекает. Поэтому нет единой и всеобъемлющей классификации встречающихся случаев коррозии.
По типу агрессивных сред, в которых протекает процесс разрушения, коррозия может быть следующих видов:
1) -Газовая коррозия
2) -Коррозия в неэлектролитах
3) -Атмосферная коррозия
4) -Коррозия в электролитах
5) -Подземная коррозия
7) -Коррозия блуждающим током.
По условиям протеканию коррозионного процесса различаются следущие виды:
1) -Контактная коррозия
2) -Щелевая коррозия
3) -Коррозия при неполном погружении
4) -Коррозия при полном погружении
5) -Коррозия при переменном погружении
6) -Коррозия при трении
7) -Коррозия под напряжением.
По характеру разрушения:
Сплошная коррозия, охватывающая всю поверхность:
Локальная(местная) коррозия, охватывающая отдельные участки:
3) -точечная(или питтинг);
1. Химическая коррозия
Представим себе металл в процессе производства металлического проката на металлургическом заводе: по клетям прокатного стана движется раскаленная масса. Во все стороны от нее разлетаются огненные брызги. Это с поверхности металла скалываются частички окалины – продукта химической коррозии, возникающего в результате взаимодействия металла с кислородом воздуха. Такой процесс самопроизвольного разрушения металла из-за непосредственного взаимодействия частиц окислителя и окисляемого металла, называется химической коррозией.
Химическая коррозия — взаимодействие поверхности металла с (коррозионно-активной) средой, не сопровождающееся возникновением электрохимических процессов на границе фаз. В этом случае взаимодействия окисление металла и восстановление окислительного компонента коррозионной среды протекают в одном акте. Например, образование окалины при взаимодействии материалов на основе железа при высокой температуре с кислородом:
4Fe + 3O 2 → 2Fe 2 O 3
При электрохимической коррозии ионизация атомов металла и восстановление окислительного компонента коррозионной среды протекают не в одном акте и их скорости зависят от электродного потенциала металла (например, ржавление стали в морской воде).
При химической коррозии окисление металла и восстановление окислительного компонента коррозионной среды происходят одновременно. Такая коррозия наблюдается при действии на металлы сухих газов (воздуха, продуктов горения топлива) и жидких не электролитов (нефти, бензина и т. д.) и представляет собой гетерогенную химическую реакцию.
Процесс химической коррозии происходит следующим образом. Окислительный компонент внешней среды, отнимая у металла валентные электроны, одновременно вступает с ним в химическое соединение, образуя на поверхности металла пленку (продукт коррозии). Дальнейшее образование пленки происходит за счет взаимной двусторонней диффузии через пленку агрессивной среды к металлу и атомов металла по направлению к внешней среде и их взаимодействия. При этом если образующаяся пленка обладает защитными свойствами, т. е. препятствует диффузии атомов, то коррозия протекает с самоторможением во времени. Такая пленка образуется на меди при температуре нагрева 100 °С, на никеле — при 650, на железе — при 400 °С. Нагрев стальных изделий выше 600 °С приводит к образованию на их поверхности рыхлой пленки. С повышением температуры процесс окисления идет с ускорением.
Наиболее распространенным видом химической коррозии является коррозия металлов в газах при высокой температуре — газовая коррозия. Примерами такой коррозии являются окисление арматуры печей, деталей двигателей внутреннего сгорания, колосников, деталей керосиновых ламп и окисление при высокотемпературной обработке металлов (ковке, прокате, штамповке). На поверхности металлоизделий возможно образование и других продуктов коррозии. Например, при действии сернистых соединений на железе образуются сернистые соединения, на серебре при действии паров йода — йодистое серебро и т. д. Однако чаще всего на поверхности металлов образуется слой оксидных соединений.
Большое влияние на скорость химической коррозии оказывает температура. С повышением температуры скорость газовой коррозии увеличивается. Состав газовой среды оказывает специфическое влияние на скорость коррозии различных металлов. Так, никель устойчив в среде кислорода, углекислого газа, но сильно корродирует в атмосфере сернистого газа. Медь подвержена коррозии в атмосфере кислорода, но устойчива в атмосфере сернистого газа. Хром обладает коррозионной стойкостью во всех трех газовых средах.
Для защиты от газовой коррозии используют жаростойкое легирование хромом, алюминием и кремнием, создание защитных атмосфер и защитных покрытий алюминием, хромом, кремнием и жаростойкими эмалями.
2. Химическая коррозия в судовых паровых котлах.
Виды коррозии. В процессе работы элементы парового котла подвергаются воздействию агрессивных сред — воды, пара и дымовых газов. Различают коррозию химическую и электрохимическую.
Химической коррозии подвержены детали и узлы машин, работающих при высоких температурах, — двигатели поршневого и турбинного типа, ракетные двигатели и т. п. Химическое сродство большинства металлов к кислороду при высоких температурах почти неограниченно, так как оксиды всех технически важных металлов способны растворяться в металлах и уходить из равновесной системы:
2Ме(т) + O 2 (г) 2МеО(т); МеО(т) [МеО] (р-р)
В этих условиях окисление всегда возможно, но наряду с растворением оксида появляется и оксидный слой на поверхности металла, который может тормозить процесс окисления.
Скорость окисления металла зависит от скорости собственно химической реакции и скорости диффузии окислителя через пленку, а поэтому защитное действие пленки тем выше, чем лучше ее сплошность и ниже диффузионная способность. Сплошность пленки, образующейся на поверхности металла, можно оценить по отношению объема образовавшегося оксида или другого какого-либо соединения к объему израсходованного на образование этого оксида металла (фактор Пиллинга-Бэдвордса). Коэффициент a (фактор Пиллинга — Бэдвордса) у разных металлов имеет разные значения. Металлы, у которых a в частности, сведения о коррозии их экранов.
Экраны этих котлов были подвержены коррозии как с наружной, так и с внутренней стороны. Их наружная коррозия описана в предыдущем параграфе этой главы, разрушение же внутренней поверхности труб не похоже ни на один из описанных выше видов коррозии металла
Разъедание происходило в основном с огневой стороны верхней части наклонных труб холодной воронки и сопровождалось появлением коррозионных раковин (рис. 63,а). В дальнейшем число таких раковин увеличивалось, и возникала сплошная полоса (иногда две параллельные. полосы) разъеденного металла (рис. 63,6). Характерным являлось также отсутствие коррозии в зоне сварных стыков.
Внутри труб имелся налет рыхлого шлама толщиной 0,1-0,2 мм, состоявшего в основном из окислов железа и меди. Увеличение коррозионного разрушения металла не сопровождалось увеличением толщины слоя шлама, следовательно, коррозия под слоем шлама не была основной причиной разъедания внутренней поверхности экранных труб.
В котловой воде поддерживался режим чистофосфатной щелочности. Фосфаты вводились в котел не.непрерывно, а периодически.
Большое значение имело то обстоятельство, что температура металла труб периодически резко.повышалась и иногда была выше 600° С (рис. 64). Зона наиболее частого и максимального повышения температуры совпадала с зоной наибольшего разрушения металла. Снижение давления в котле до 140-165 ат (т. е. до давления, при котором работают новые серийные котлы) не изменяло характера временного повышения температуры труб, но сопровождалось значительным снижением максимального значения этой температуры. Причины такого периодического повышения температуры огневой стороны наклонных труб холодной. воронки еще подробно не изучены.

В настоящей книге рассматриваются конкретные вопросы, связанные с работой стальных деталей парового котла. Но для изучения этих сугубо практических вопросов необходимо знать общие сведения, касающиеся строения стали и ее » свойств. В схемах, показывающих строение металлов, атомы иногда изображают в виде соприкасающихся друг с другом шаров (рис. 1). Такие схемы показывают расстановку атомов в металле, но в них трудно наглядно показать расположение атомов друг относительно друга.
Эрозией называется постепенное разрушение поверхностного слоя металла под влиянием механического воздействия. Наиболее распространенным видом эрозии стальных элементов — парового котла является их истирание твердыми частицами золы, движущейся вместе с дымовыми газами. При длительном истирании происходит постепенное уменьшение толщины стенок труб, а затем их деформация и разрыв под действием внутреннего давления.
Коррозия экранных труб паровых котлов. Наружная коррозия экранных труб. Обработка котловой воды
Наиболее активно коррозия экранных труб проявляется в местах концентрирования примесей теплоносителя. Сюда относятся участки экранных труб с высокими тепловыми нагрузками, где происходит глубокое упаривание котловой воды (особенно при наличии на испарительной поверхности пористых малотеплопроводных отложений). Поэтому в отношении предупреждения повреждений экранных труб, связанных с внутренней коррозией металла, нужно учитывать необходимость комплексного подхода, т.е. воздействия как на водно-химический, так и топочный режим.
Повреждения экранных труб в основном носят смешанный характер, их условно можно разделить на две группы:
1) Повреждения с признаками перегрева стали (деформация и утонение стенок труб в месте разрушения; наличие графитных зерен и т.д.).
2) Хрупкие разрушения без характерных признаков перегрева металла.
На внутренней поверхности многих труб отмечены значительные отложения двухслойного характера: верхний — слабосцепленный, нижний — окалинообразный, плотно сцепленный с металлом. Толщина нижнего слоя окалины составляет 0.4-0.75 мм. В зоне повреждения окалина на внутренней поверхности подвергается разрушению. Вблизи мест разрушений и на некотором удалении от них внутренняя поверхность труб поражена коррозионными язвинами и хрупкими микроповреждениями.
Общий вид повреждений свидетельствует о тепловом характере разрушения. Структурные изменения на лобовой стороне труб — глубокая сферидизация и распад перлита, образование графита (переход углерода в графит 45-85%) — свидетельствует о превышении не только рабочей температуры экранов, но и допустимой для стали 20 500 оС. Наличие FeO также подтверждает высокий уровень температур металла в процессе эксплуатации (выше 845 оК — т.е. 572 оС).
Хрупкие повреждения, вызванные водородом, обычно происходят в зонах с мощными тепловыми потоками, под толстыми слоями отложений, и на-клонных или горизонтальных трубах, а также на участках теплопередачи рядом с подкладными кольцами сварных швов либо другпмии устройства-ми, препятствующими свободному движению потоков..Опыт показал, что повреждения, вызванные водородом, происходят в котлах, работающих под давлением ниже 1000 фунт/кв. дюйм (6.9 МПа).
Повреждення под действием водорода обычно приводят к разрывам с тол-стыми краями. Другие механизмы, способствующие образованию разры-вов с толстыми краями, это коррозионное растрескивание под напряжени-ем, коррозионная усталость, разрывы под действием напряжений, а также (в некоторых редких случаях) сильнейший перегрев. Может оказаться за-труднительным визуально отличить разрушения, вызванные водородным повреждением, от других видов разрушений, однако здесь могут помочь не-которые их особенности.
Например, водородное повреждение почти всегда связано с образова-нием раковин в металле (см. меры предосторожности, приведенные в Гла-вах 4 и 6). Другие виды разрушений (за исключением, возможно, коррози-онной усталости, которая часто начинается в отдельных раковинах) обыч-но не связаны с сильной коррозией.
Аварии труб в результате водородного повреждения металла часто про-являются в виде образования в стенке трубы прямоугольного «окна», что не характерно для других видов разрушений.
Для оценки повреждаемости экранных труб следует учитывать, что металлургическое (исходное) содержание газообразного водорода в стали перлитного класса (в т.ч. ст.20) не превышает 0.5—1 см3/100г. При содержании водорода выше 4—5 см3/100г механические свойства стали существенно ухудшаются. При этом ориентироваться надо преимущественно на локальное содержание остаточного водорода, поскольку при хрупких разрушениях экранных труб резкое ухудшение свойств металла отмечается только в узкой зоне по сечению трубы при неизменно удовлетворительных структуре и механических свойствах прилегаемого металла на удалении всего 0.2-2мм.
Полученные значения средних концентраций водорода у кромки разрушения в 5-10 раз превышают его исходное содержание для ст.20, что не могло не оказать существенного влияния на повреждаемость труб.
Приведенные результаты свидетельствуют, что водородное охрупчивание оказалось решающим фактором повреждаемости экранных труб котлов КрТЭЦ.
Потребовалось дополнительное изучение, какой из факторов оказывает на этот процесс определяющее влияние: а) термоциклирование из-за дестабилизации нормального режима кипения в зонах повышенных тепловых потоков при наличии отложений на испарительной поверхности, а, как результат, — повреждение покрывающих ее защитных оксидных пленок; б) наличие в рабочей среде коррозионно активных примесей, концентрирующихся в отложениях у испарительной поверхности; в) совместное действие факторов «а» и «б».
Особо стоит вопрос о роли топочного режима. Характер кривых свидетельствует о скоплении водорода в ряде случаев вблизи наружной поверхности экранных труб. Это возможно прежде всего при наличии на указанной поверхности плотного слоя сульфидов, в значительной мере не проницаемых для водорода, диффундирующего от внутренней поверхности к наружной. Образование сульфидов обусловлено: высокой сернистостью сжигаемого топлива; набросом факела на экранные панели. Другой причиной наводораживания металла у наружной поверхности является протекание коррозионных процессов при контакте металла с дымовыми газами. Как показал анализ наружных отложений труб котлов, обычно имело место действие обеих приведенных причин.
Роль топочного режима проявляется также в коррозии экранных труб под действием чистой воды, которая чаще всего наблюдается на парогенераторах высокого давления. Очаги коррозии расположены обычно в зоне максимальных местных тепловых нагрузок и только на обогреваемой поверхности трубы. Это явление ведет к образованию круглых или эллиптических углублений диаметром больше 1 см.
Перегрев металла возникает наиболее часто при наличии отложений в связи с тем, что количество воспринятого тепла будет практически одинаковым как для чистой трубы, так и для трубы, содержащей накипь температура трубы будет разной.
МИНИСТЕРСТВО ЭНЕРГЕТИКИ И ЭЛЕКТРИФИКАЦИИ СССР
ГЛАВНОЕ НАУЧНО-ТЕХНИЧЕСКОЕ УПРАВЛЕНИЕ ЭНЕРГЕТИКИ И ЭЛЕКТРИФИКАЦИИ
МЕТОДИЧЕСКИЕ УКАЗАНИЯ
ПО ПРЕДУПРЕЖДЕНИЮ
НИЗКОТЕМПЕРАТУРНОЙ
КОРРОЗИИ ПОВЕРХНОСТЕЙ
НАГРЕВА И ГАЗОХОДОВ КОТЛОВ
РАЗРАБОТАНО Всесоюзным дважды ордена Трудового Красного Знамени теплотехническим научно-исследовательским институтом имени Ф.Э. Дзержинского
ИСПОЛНИТЕЛИ Р.А. ПЕТРОСЯН, И.И. НАДЫРОВ
УТВЕРЖДЕНО Главным техническим управлением по эксплуатации энергосистем 22.04.84 г.


